Representación artística de como la lateralidad molecular surgió en la biología temprana. Crédito de la imagen: Pexels
Las moléculas tienen con frecuencia una asimetría estructural llamada quiralidad, lo que significa que pueden aparecer en versiones alternativas, como reflejadas en un espejo, similares a las versiones izquierda y derecha de las manos humanas. La aparición de prácticamente todas las moléculas fundamentales de la biología, como los componentes básicos de las proteínas y el ADN, en una sola forma quiral es uno de los grandes misterios sobre el origen de la vida en la Tierra.
En dos estudios destacados, los químicos de Scripps Research han sugerido una solución ingeniosa a este misterio, demostrando cómo esta singularidad u «homoquiralidad» podría haber surgido en biología.
La investigación fue publicada en Nature y en las Actas de la Academia Nacional de Ciencias. Juntos, sugieren que la resolución cinética, un fenómeno químico en el que una forma quiral se vuelve más abundante que otra debido a una producción más rápida y/o un agotamiento más lento, es la causa principal de la homoquiralidad.
Donna Blackmond, Ph.D., profesora y catedrática de John C. Martin en el Departamento de Química de Scripps Research, quien dirigió ambos estudios, comentó: «Ha habido muchas propuestas sobre cómo surgió la homoquiralidad en moléculas específicas (por ejemplo, aminoácidos específicos), pero realmente necesitábamos una teoría más general».
Los primeros autores de los dos estudios fueron Jinhan Yu, un estudiante de posgrado, y Min Deng, Ph.D., un investigador postdoctoral asociado.
El enigma de la homoquiralidad
Durante gran parte del siglo pasado, la química del «origen de la vida» ha sido un campo muy activo. Sus especialistas han descubierto numerosas reacciones cruciales que podrían haber ocurrido en la Tierra primitiva y «prebiótica» para generar los primeros ADN, ARN, azúcares, aminoácidos y otras moléculas esenciales para la supervivencia. No obstante, en este conjunto de estudios no se presenta una teoría prebiótica convincente para la aparición de la homoquiralidad
Blackmond afirma que cuando se buscan reacciones plausibles que podrían haber formado las primeras moléculas biológicas, hubo una tendencia en el campo a ignorar el problema de la quiralidad. Es frustrante porque no tendríamos vida sin reacciones que fomenten la homoquiralidad.
Las mezclas iguales («racémicas») de formas diestras y zurdas suelen resultar de reacciones químicas comunes que producen moléculas quirales. Dado que ambas formas suelen tener características similares o idénticas, esta mezcla normalmente no importa en la biología.
No obstante, en biología, debido a la gran homoquiralidad, es común que solo la forma izquierda o derecha de una molécula quiral tenga características beneficiosas, mientras que la otra puede ser inerte o incluso peligrosa. Por lo tanto, las células con frecuencia utilizan enzimas altamente evolucionadas para guiar reacciones para producir formas quirales específicas.
Sin embargo, la Tierra prebiótica no habría tenido tales enzimas. Entonces, ¿Cómo surgió la homoquiralidad?
Un resultado sorprendente.
Blackmond y su equipo resolvieron el problema de los aminoácidos en un estudio que publicaron en Proceedings of the National Academy of Sciences. Todos los seres vivos de la Tierra utilizan estas pequeñas moléculas orgánicas como componentes básicos de proteínas, pero en biología solo se encuentran en su forma quiral izquierda.
Con el uso de una química relativamente simple y probablemente prebiótica que excluye enzimas complejas, los investigadores buscaron específicamente reproducir la homoquiralidad en un proceso central en la producción de aminoácidos llamado transaminación.
La reacción experimental del equipo funcionó en las primeras pruebas, produciendo aminoácidos enriquecidos para una forma quiral frente a la otra. El problema radicaba en que la forma preferida era la derecha, que no se utiliza en biología.
Blackmond afirma: «Estuvimos estancados por un tiempo, pero luego tuvimos una idea y nos dimos cuenta de que podíamos participar en la reacción a la inversa».
Después de hacer eso, la reacción ya no produjo aminoácidos diestros. En un ejemplo asombroso de resolución cinética, en cambio, prefirió consumir y agotar las versiones diestras, lo que dejó más aminoácidos zurdos deseados. Como resultado, proporcionó un camino razonable hacia la homoquiralidad de los aminoácidos utilizados en las células vivas.
Combinar todo.
aminoácidos de las primeras formas de vida se unieran para formar los primeros péptidos. Otro investigador había publicado un estudio sobre la reacción, pero nunca se había estudiado por su capacidad para producir péptidos homoquirales a partir de mezclas de aminoácidos racémicos o casi racémicos.
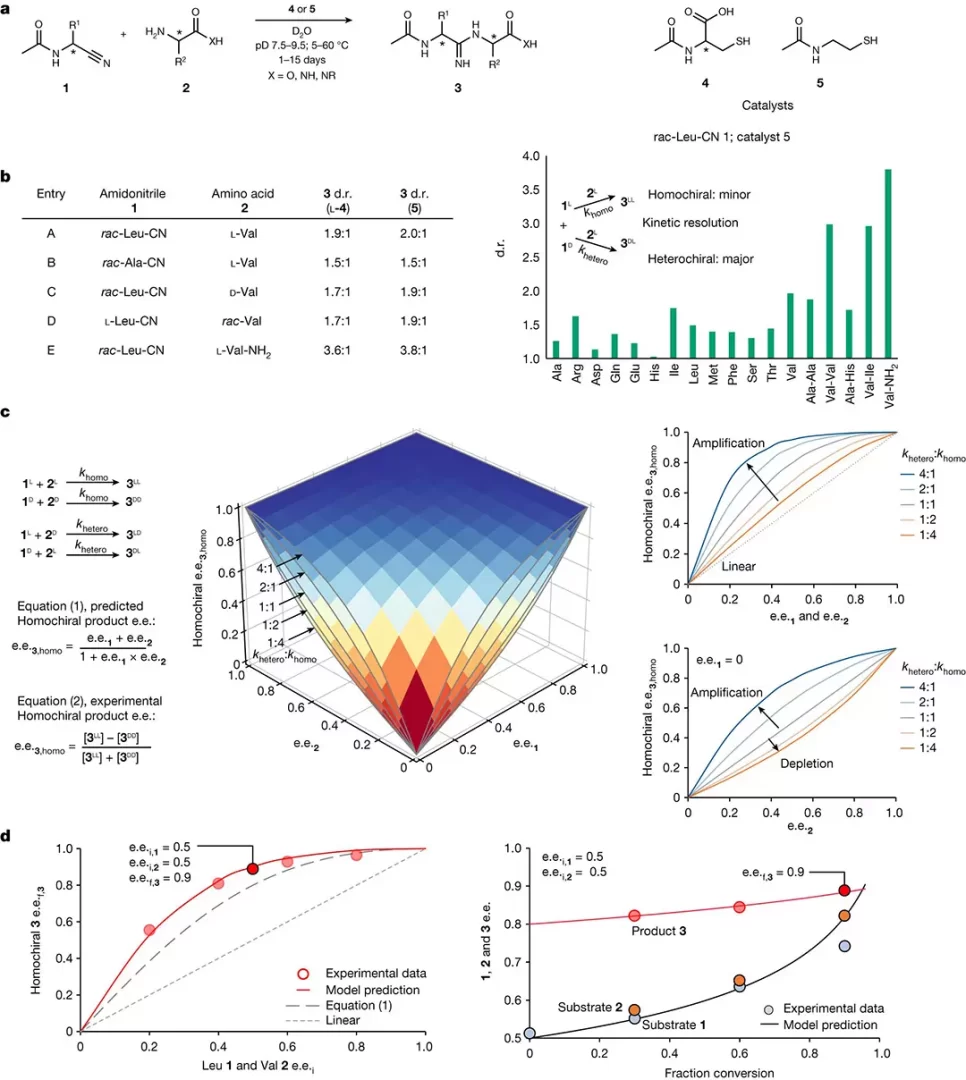
Los químicos encontraron una vez más lo que parecía ser un obstáculo insuperable: al formar cadenas peptídicas de aminoácidos, la reacción funcionaba más rápido para los enlaces de aminoácidos zurdos con aminoácidos diestros, en lugar de los péptidos homoquirales deseados.
El equipo persistió. Al final, descubrieron que cuando un tipo de aminoácido en el grupo inicial de aminoácidos tenía incluso un predominio moderado de la forma zurda (como su otro estudio hizo plausible), los zurdos y los diestros tenían mayores velocidades de reacción. Los enlaces diestros agotan los aminoácidos diestros con mayor frecuencia, lo que aumenta la concentración de aminoácidos zurdos.
Además, se observó una mayor tendencia de los péptidos de izquierda-derecha-izquierda-derecha a agruparse y salir de la solución en forma sólida. Estos fenómenos de resolución cinética produjeron una solución sorprendentemente pura de péptidos casi completamente zurdos.
Blackmond cree que los mecanismos aparentemente paradójicos descubiertos en estos estudios brindan la primera explicación convincente y completa del surgimiento de la homoquiralidad. Según él, esta explicación probablemente sea efectiva no solo para los aminoácidos, sino también para otras moléculas fundamentales de la biología, como el ADN y el ADN. ARN
REFERENCIAS
Prebiotic access to enantioenriched amino acids via peptide-mediated transamination reactions. Proceedings of the National Academy of Sciences: https://www.pnas.org/doi/10.1073/pnas.2315447121
Symmetry breaking and chiral amplification in prebiotic ligation reactions. Nature: https://www.nature.com/articles/s41586-024-07059-y
Publicaciones Relacionadas:
Publicaciones no Relacionadas.



